近日,我校材料科学与工程学院刘昌胜院士团队在干细胞治疗研究方面取得新进展,相关研究成果以“Insitu licensing of mesenchymal stem cell immunomodulatory function via BMP-2induced developmental process”为题,发表在《美国国家科学院院刊》(PNAS)上。
间充质干细胞(MSCs)因其卓越的免疫调节功能、低免疫原性和多向分化潜能,在克罗恩病、移植物抗宿主病、系统性红斑狼疮等多种炎症性疾病的治疗中具有重要价值。研究表明,当MSCs被招募到炎症部位时,功能会受到周围免疫细胞的影响,一般需通过炎症因子预处理MSCs,以增强其免疫调节能力。但这种预处理会导致MSC失去免疫豁免权,容易被宿主免疫系统清除,且预处理后的功能增强随着时间延长逐渐下降,限制了其临床应用。
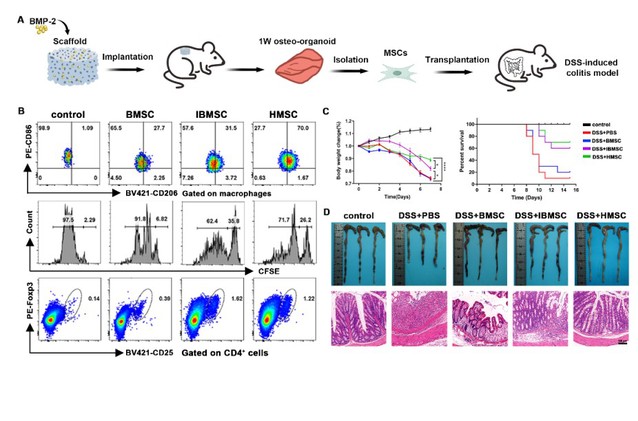
为解决这一问题,研究团队提出了一种新型的“自体MSC原位授权”策略,通过植入负载骨形态发生蛋白2(BMP-2)的生物活性材料在体内构建类骨组织,借助发育早期的炎性微环境来激活MSCs的免疫调节功能。研究表明,该方法所获得的自体MSCs具有更低的免疫原性,有助于其在宿主中的长期存活,且更长时间保持其免疫调节能力。这些优异的免疫调节特性使其在小鼠溃疡性结肠炎的治疗中获得显著的效果,降低死亡率,重塑结肠部位炎症生态位。这种由植入活性材料而产生的自体来源MSC为干细胞治疗提供了一种有前景的全新细胞来源。
我校材料科学与工程学院博士生朱富威为论文第一作者,我校王靖教授、刘昌胜教授为通讯作者。该研究工作得到了国家自然科学基金基础科学中心项目、国家自然科学基金重点项目、材料生物学与动态化学前沿科学中心和国家自然科学基金青年科学基金的支持。
原文链接:https://www.pnas.org/doi/10.1073/pnas.2410579121






